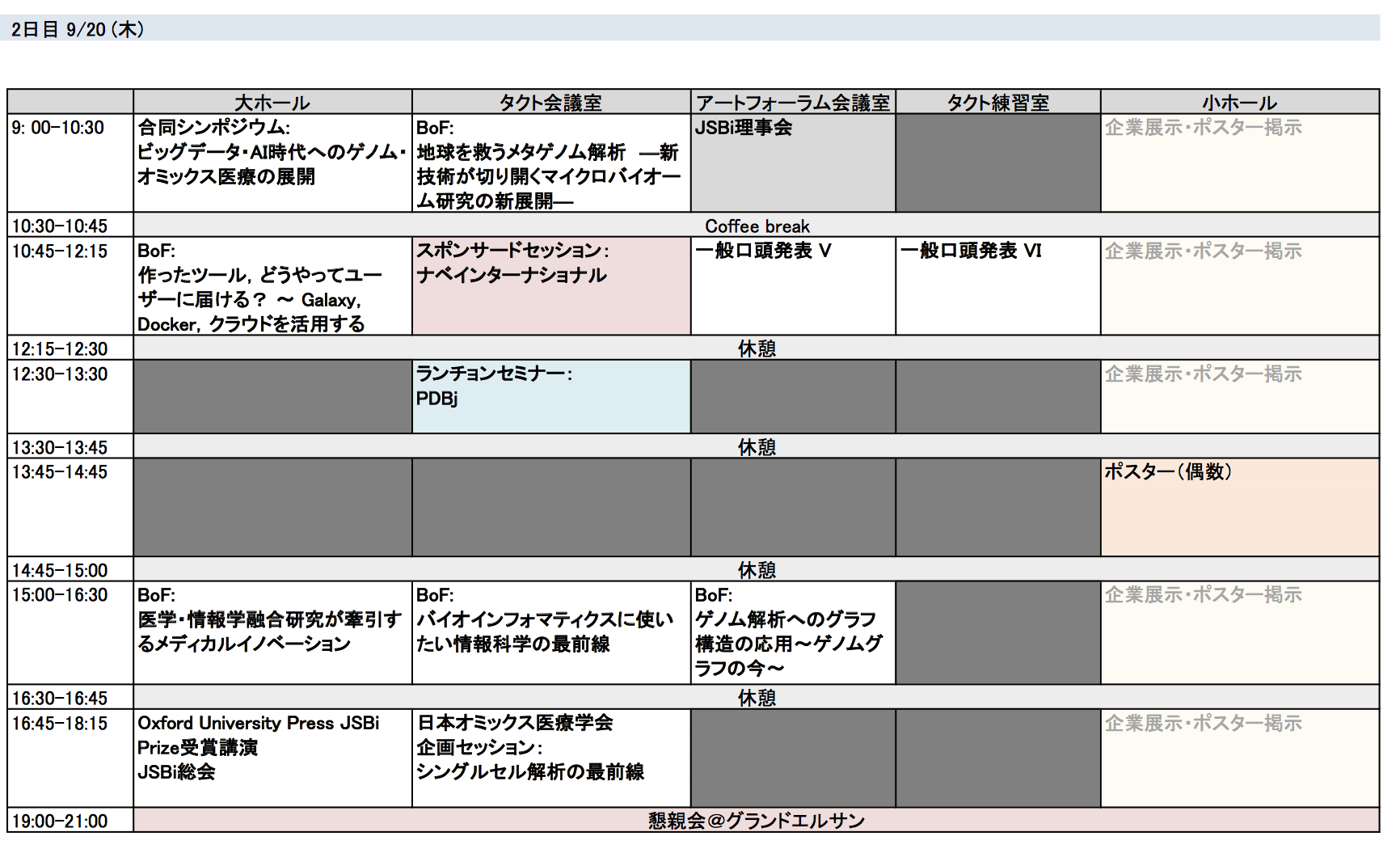
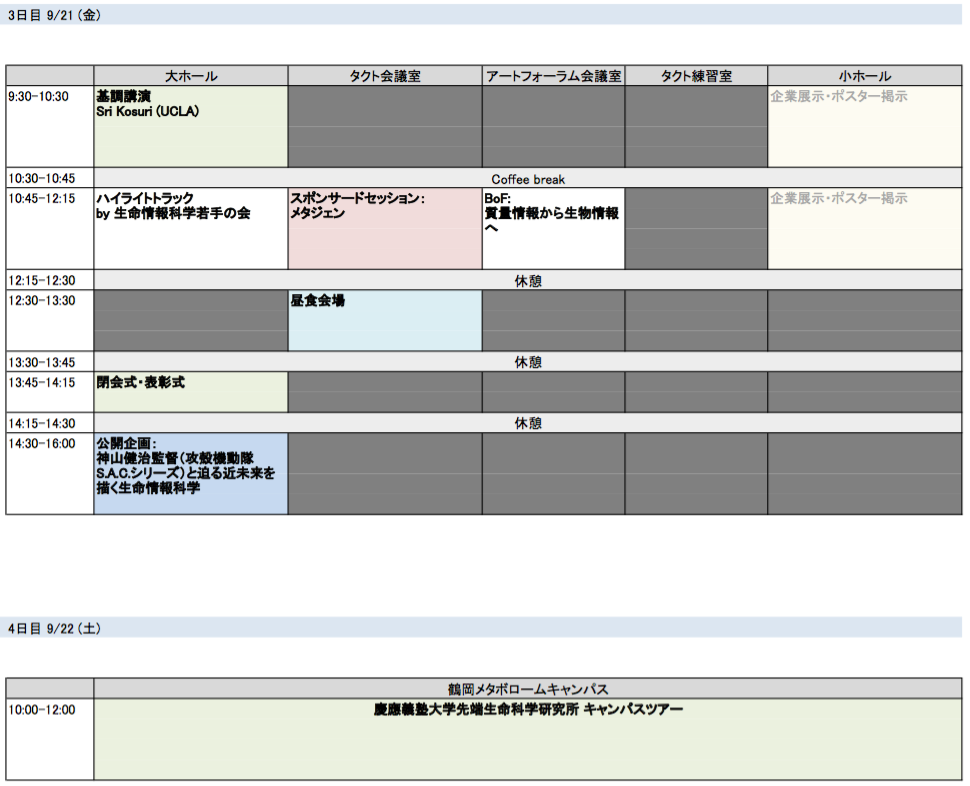
タイムテーブル
基調講演
Combining Large-scale Gene Synthesis and Multiplexed Assays to Explore Protein Function
講演者:Sri Kosuri (UCLA)

The ability to build and functionally test DNA sequences is central to molecular biology and genetic engineering. Our laboratory attempts to scale this process by developing methods in gene synthesis and multiplexed functional assays to build and test hypotheses with orders of magnitude increased scale. I will first talk about a new gene synthesis technology called DropSynth that allows for the facile synthesis of gene libraries for vastly reduced costs to characterize protein functional landscapes. I will then discuss our recent development of multiplexed functional assays for G-protein coupled receptor activity in human cell lines. I will describe our use of this system to explore ligand-receptor interactions at unprecedented scale to examine mammalian olfactory receptors and human drug targets.
プレナリー講演
マルチオミクスによるがんの代謝解明
講演者:曽我朋義(慶應義塾大学先端生命科学研究所)

曽我教授は世界に先駆けてキャピラリー電気泳動-質量分析計(CE-MS)によるメタボローム測定法を開発されました。現在は、本法を用いて微生物、植物、哺乳動物、ヒトの細胞、組織や培養細胞等の代謝産物を網羅的に測定し、新規代謝経路の探索、代謝調節機構の解明、遺伝子、タンパク質の機能解明などの学術研究から、がんの代謝や疾患の機序の解明、各種のバイオマーカー探索等の応用研究を展開されています。第5回バイオビジネスコンペJAPAN最優秀賞(2005年)、平成21年度全国発明表彰 発明協会会長賞(2009年)、慶應義塾賞(2011年)、寺部茂賞(2015年)など受賞多数。
公開企画
神山健治監督(『攻殻機動隊 S.A.C.』シリーズ)と迫る近未来を描く生命情報科学
特別ゲスト:神山健治監督(『攻殻機動隊 S.A.C.』シリーズ、『東のエデン』、『ひるね姫〜知らないワタシの物語〜』ほか)
司会:河野暢明(慶應義塾大学先端生命科学研究所)
モデレーター:秋山泰(東京工業大学),荒川和晴(慶應義塾大学先端生命科学研究所)

神山健治監督は『攻殻機動隊S.A.C.』シリーズ、『009 RE:CYBORG』、『ひるね姫〜知らないワタシの物語〜』など多くの大人気作品のアニメーション映画監督として知られ、これまでに手がけた作品はそのどれもが後続の世代に大きな影響を及ぼしています。特に攻殻機動隊S.A.C.シリーズの世界観は綿密な科学考証によって裏打ちされており、現代の生命科学分野が抱える問題と深くつながる点も多く、本作品を題材に思考実験した生命情報学者は少なくありません。本公開企画ではそんな神山健治監督をゲストに迎え、東京工業大学秋山泰教授、慶應義塾大学荒川和晴准教授がモデレーターとなり、近未来に向けて生命情報科学が担うべき課題や、実現すべき夢についてトークします。
※こちらは一般公開企画となります。9月21日(金)14:30-16:00の本企画のみ、一般市民の方を含め、参加登録なしでご参加いただけます。当日直接会場までお越し下さい。
合同シンポジウム
ビッグデータ・AI時代へのゲノム・オミックス医療の展開
座長:荻島創一(東北大学東北メディカル・メガバンク機構ゲノム医療情報学分野)
・ビッグデータ医療・創薬における人工知能(AI)の展望
田中博(東京医科歯科大学)
近年、バイオテクノロジーの急速な発展を受けて、医療・創薬分野も「ビッグデータ」時代を迎えた。これに伴い、生命情報や化合物情報のビッグデータに基づいて、ディープラーニング(深層学習)などの人工知能(AI)を用いて、医療分野における応用や、生体ビッグデータが持つ「創薬力」を抽出し、疾患の薬剤標的分子の探索、標的分子へ化合物のバーチャルスクリーニングや既存薬のドラッグリポジショニング(DR)を目指す「AI創薬・DR」の研究が進展している。
本講演では、ビッグデータ医療やAI創薬・DRについて、現在の研究をできるだけ体系的・俯瞰的に紹介する。すなわち、医療においては、深層学習が得意とする、人の「教師あり学習」の助けを借りずに自動的にデータ内在的な特徴抽出する機能が、ゲノム・オミックス解析、モバイルヘルスにおける信号処理、電子カルテ情報の自動認識、公衆衛生分野などの分野でどのように生かされているかを総攬する。またAI創薬の分野では「疾病-薬剤(化合物)-生体システム」の3階層ネットワークを基本的枠組みとして、ヒトのタンパク質相互作用ネットワークを生体システムモデルとする「生体分子プロファイル型創薬基礎論」を土台として、とくに、最近注目されている「ネットワーク埋め込み(Network Embedding)」理論を基礎として、ディープラーニングによって自動化する初期創薬パイプラインの可能性に関して、実例を交えて体系的に述べる。
・人工知能技術の医療応用への展開と展望
瀬々潤(株式会社ヒューマノーム研究所 / 社団法人日本メディカルAI学会 / 産業技術総合研究所 人工知能研究センター)
最近、毎日の様に人工知能(AI)に関する論文や記事を見かける。その中でも医療に関する記事は多く、よりよい医療に関する社会的な期待を感じる。一方で、報道では同じ様な書き方をされているものでもレベル感は様々で、単にテストして成功しましたという研究初期のものから、機器としてあるいは検査手法として認可を受けましたというものもある。更には、時間が経つにつれ、AIの応用は必ずしも期待通りにいかず、失敗事例のように報道されるケースも出てきた。過度な期待は難しくとも、生命情報研究者としては、今まで基礎研究でとどまることの多かった現状から、ある種の’応用につながる道が出てきたことは喜ばしい。本講演では、現状の多様なオミックス情報の医療応用の現状を人工知能技術の観点から俯瞰し、演者が関係する医療系プロジェクトの実例を紹介する。その上で、今後のバイオインフォマティクス・マルチオミックス、それらに人工知能が加わることで、今後の健康・医療への展開をどのように行っていくか、ディスカッションを行いたい。
・リアルワールドデータである医療情報の二次利用による病態分類(フェノタイピング)とゲノム・オミックス医療への展開
荻島創一 (東北大学東北メディカル・メガバンク機構ゲノム医療情報学分野)
個々人のゲノムに基づくゲノム医療の研究開発が進展するなかで、遺伝型については精度の高い高深度のゲノム情報が産生される一方、表現型の情報についても、病名のみならず、より精度の高い高深度の情報が必要となってきている。こうしたなか、リアルワールドデータである医療情報のビッグデータを二次利用して、病態の情報を得ることが重要となっている。医療情報の二次利用による病態分類(フェノタイピング)の現状と動向について紹介する。こうして得られた病態情報は、ゲノム・オミックス情報と連結して、ゲノム・オミックス医療の研究開発に利用することが期待される。
日本オミックス医療学会企画セッション
シングルセル解析の最前線
座長:岡﨑康司(順天堂大学難病の診断と治療研究センター)
・1細胞トランスクリプトームとその情報解析技術の最前線
二階堂愛(理化学研究所生命機能科学研究センターバイオインフォマティクス研究開発ユニット / 筑波大学グローバル教育院ライフイノベーション学位プログラム生物情報領域)
生命現象を理解する上で、細胞集団の不均質性を知ることは非常に重要である。不均質性の検出を求められる課題は、初期発生や器官形成、細胞分化、ガン幹細胞、体性幹細胞など希少細胞同定など、多岐にわたる。1細胞RNAシーケンス法は、これらの不均質性を知る上で最も包括的かつ有効な手段の1つである。近年、1細胞RNAシーケンス技術は急速に発展し、計測可能な細胞処理数と遺伝子検出感度が大幅に改善した(Sasagawa Y. et al. 2018)。さらに、非ポリA型RNAや長鎖RNA全長を捉えられる1細胞トータルRNAシーケンス法も登場し、1細胞レベルでのRNA配列変異を捉えられるようになった(Hayashi T et al. 2018)。同時に、このようなデータを活用するには、高度な情報解析が必要である(Tsuyuzaki K. et al. 2018)。特に、細胞分化系譜・時間・速度や転写制御ネットワーク予測(Matsumoto H. et al. 2017)、細胞類似検索(Sato K et al. under review)、細胞空間配置予測法などの開発が行われてきた。本講演では、我々が取り組んできた1細胞シーケンス法とそれらを活かす情報科学的手法について報告する。さらに、今後、1細胞シーケンス解析をオミックス医療に活かす上で、生命情報科学分野にどのような発展が期待されるかを議論したい。
・シングルセル遺伝子発現解析で迫る細胞運命決定機構
渡辺 亮(京都大学 iPS細胞研究所 未来生命科学開拓部門)
生体を構成する最小単位である一細胞レベルでの遺伝子発現解析(single cell RNA-sequencing, scRNA-seq)は、細胞の多様性と階層性を解析するツールとして広く行われている。我々は分子レベルで転写制御を理解するために、scRNA-seqのデータを用いることで、転写制御の最小単位である一アリルレベルでの解析を実施した。まず、ヒトiPS細胞に対して実施した全ゲノムシークエンシング及びSNPアレイ解析よりヘテロSNPの検出を行った。そして、cDNA全長を対象としたシングルセル遺伝子発現解析で得られたシークエンスリードに対して、転写産物のSNPコールを実施した。細胞集団を対象にしたRNAシークエンシングのデータを解析した結果、多くの遺伝子は両アリルからの発現であったが、シングルセルレベルでは大多数が片側のアリルからの発現を示していた。一方で、特定の遺伝子に注目した場合、個々の細胞における使用アリルは一定でない傾向が得られた。全ての細胞で父性アリルあるいは母性アリルのいずれかから発現するstably mono-allelic expressionを示す遺伝子あるいは、全ての細胞で両アリルから発現するstably bi-allelic expressionを示す遺伝子はわずかであったが多能性を制御している遺伝子が含まれていた。この結果は、個々の細胞におけるアリル使用は基本的にランダムに行われているが、その分化制御に関わる厳密な制御も含まれていることを示唆している。
・The single cell PBMC transcriptome of supercentenarians
Kosuke Hashimoto (RIKEN Center for Integrative Medical Sciences)
The supercentenarian, over age 110, is a great model of healthy ageing. We aim to understand the ageing process in the later stage of life using technologies for transcriptome analysis. Here we report our results of the single cell transcriptome analysis on peripheral blood mononuclear cells (PBMC), derived from Japanese supercentenarians and younger controls. In total, 60,000 single cells from 12 donors were profiled using 10X Genomics single cell libraries. We identified major cell types in PBMCs, including T cells characterized by the expression of CD3, B cells characterized by CD20, NK cells, and monocytes as well as 3 small clusters, annotated as MKI67 positive proliferating cells, dendritic cells, and megakaryocytes. Among the major cell types, B cells are significantly reduced in supercentenarians mainly due to the loss of naive B cells, whereas other cell types including T-cells are not clearly changed. However, T-cell subtypes are largely shifted from non-cytotoxic to cytotoxic in supercentenarians, contributed by both CD4 and CD8 positive T-cells, suggesting dynamic shift of lymphocyte population might play roles in exceptional longevity.
ハイライトトラック
ハイライトトラック by 生命情報科学若手の会
座長:河野暢明(慶應義塾大学先端生命科学研究所)
・Comparative genomics of the tardigrades Hypsibius dujardini and Ramazzottius varieornatus. (PLoS Biology 2017)
吉田祐貴(慶應義塾大学先端生命科学研究所)
・MitoFish and MiFish Pipeline: A Mitochondrial Genome Database of Fish with an Analysis Pipeline for Environmental DNA Metabarcoding (Mol. Biol. Evol. 2018)
佐藤行人(琉球大 研究推進機構 戦略的研究プロジェクトセンター)
・MEGADOCK-Web: an integrated database of high-throughput structure-based protein-protein interaction predictions. (BMC Bioinformatics 2018)
大上雅史(東京工業大学 情報理工学院 情報工学系)
・MP-LAMP: Parallel Detection of Statistically Significant Multi-Loci Markers on Cloud Platforms. (Bioinformatics, 2018)
美添一樹(Advanced Intelligence Project, RIKEN)
・Genome of the pitcher plant Cephalotus reveals genetic changes associated with carnivory. (Nature Ecology and Evolution, 2017)
福島健児(理化学研究所 環境資源科学研究センター、University of Colorado Denver)
BoFセッション
地球を救うメタゲノム解析 ―新技術が切り開くマイクロバイオーム研究の新展開―
座長:西村陽介(東京大学大気海洋研究所),平岡聡史(海洋研究開発機構)
微生物群集のDNAを直接抽出してショットガンシーケンシングを行う、いわゆるメタゲノム解析は、難培養性の系統を含む細菌・古細菌の生態にゲノム情報から迫る手法として非常に有用である。近年のシーケンシング技術の飛躍的な発展により、ますます大量のDNA情報を得ることが可能になり、より「深い」シーケンシングが可能になってきた。その一方で、PacBioのような1分子シーケンサーの普及、あるいはシングルセル解析や10X Chromium systemのような新しい技術の登場により、ショットガンシーケンシングから得られるデータは「質」の面でも大きく幅が広がりつつある。同時に、メタボロミクスによる代謝物情報との統合的な解析や、ウイルスに焦点を合わせたメタゲノム解析(virome)の進展も相まって、「メタゲノム解析」の枠組みは今大きな転換の時期に来ているように感じられる。本セッションでは、新しい技術や手法を積極的に取り入れ、既存のメタゲノム解析の枠を大きく飛び出した気鋭の研究者にご講演いただき、今後の展望と可能性について議論していきたい。
・メタエピゲノム解析から迫る環境細菌・古細菌のエピジェネティクス
平岡聡史、岡崎友輔、按田瑞恵、豊田敦、中野伸一、岩崎渉
・Diverse syntrophic catabolism for escaping thermodynamic limitations
Masaru K. Nobu, Takashi Narihiro, Wen-Tso Liu
・10X Chromium systemのメタゲノム解析への応用
梶谷嶺、小椋義俊、後藤恭宏、豊田敦、林哲也、伊藤武彦
・海洋におけるウイルス生態系の理解へ向けて
西村陽介、吉田天士、五斗進、緒方博之
作ったツール,どうやってユーザーに届ける? 〜 Galaxy,Docker,クラウドを活用する
座長:志波優(東京農業大学),鈴木治夫(慶應義塾大学)
近年の生命・医薬分野では、測定技術の急速な発展により、常により優れたデータ解析手法が求められている。生命情報科学分野では、新しい種類のデータを解析するためのアルゴリズムや統計手法、既存ツールを組み合わせたワークフローの開発が行われているが、新たな手法を提案するにあたって、手法を実装したソフトウェア (ツール) をユーザに提供する必要がある。従来は開発者がインターネットを通じてツールのソースコードを公開し、ユーザは自らビルドすることが一般的であった。しかし、計算機環境の多様化と扱うツールの数の増大により、新規ツールの導入は容易ではない。そこで現在では、この問題を解決するために、統合解析環境に組み込む、コンテナ仮想化技術を用いて導入を簡易化する、クラウド上に予め実行環境を用意しておく、などの手段によってツールの利便性を高める試みが増えている。本セッションでは、統合データ解析環境 Galaxy のユーザコミュニティ(http://wiki.pitagora-galaxy.org/; twitter: @pitagora_meetup) メンバーである演者らによる事例紹介を通して、ユーザにツールを届けるために開発者が実施すべき手段について議論する。
・細菌叢解析ツールの共有~Dockerコンテナ~
菅波麻衣, 中岡慎治(東京大学)
・Galaxy にツールを実装・公開するまでの流れ
志波優(東京農業大学)
・Galaxy のインターフェースを XML で記述する
池田誠(合同会社パーシピア)
・変異解析パイプラインを Galaxy Docker で提供する
新海典夫(産業技術総合研究所)
・作成した Galaxy のワークフローを公開・共有する
山中遼太(オラクル・タイランド)
・クラウド環境で Galaxy を利用する
那須野淳(株式会社アスケイド)
・ワークフローを Common Workflow Language で記述する
丹生智也(国立情報学研究所)
・使い捨てクラウドで「今日だけ」そのワークフローを試す方法
落合展(国立がん研究センター)
医学・情報学融合研究が牽引するメディカルイノベーション
座長:島村徹平(名古屋大医学部),新井田厚司(東京大学医科学研究所)
昨今、医学研究分野においては、次世代シークエンサーや質量分析器等のハイスループット実験機器開発によって未曾有の爆発的データ増加を経験し、情報解析の重要性はますます増している。また深層学習に代表されるような新しい情報解析技術の開発も進展し、それらの医療情報への応用も進められている。今後、医学研究分野における科学的発見、技術開発および、それらの医療応用を推進して行くためには、医学と情報学、両分野に精通する人材の育成および異分野融合研究体制の確立が急務である。しかしながら、国内においてはそのような人材育成及び研究体制の確立が十分なされているとは言い難い。本セッションにおいては、医学と情報学の境界領域において活躍している研究者が最新の知見及び異分野融合研究の魅力を紹介するとともに、当該領域の若手研究者の新規参入のきっかけを提供する。
・ゲノムデータを用いた疾患原因変異の同定と疾患発症予測モデル開発の現在
重水大智(国立長寿医療研究センター メディカルゲノムセンター、東京医科歯科大学 難治疾患研究所、理化学研究所 生命医科学研究センター )
・がんゲノムにおけるスプライシング変異の網羅的な検出
白石友一 (国立がん研究センター がんゲノム情報管理センター)
・腫瘍内不均一性の中立性の判定問題
新井田厚司 (東京大学 医科学研究所)
・遺伝子系図情報を用いたシークエンスデータ解析と深層学習を用いた皮膚病理画像解析について
小島要(東北大学 東北メディカル・メガバンク機構)
・疾患メタゲノム解析のためのベイズモデリング
島村徹平、阿部興(名古屋大学大学院医学系研究科)
バイオインフォマティクスに使いたい情報科学の最前線
座長:尾崎遼(理化学研究所),福永津嵩(東京大学)
バイオインフォマティクスは生命科学と情報科学の融合分野であり、新たな生物学の問題に情報科学を適用する事や、また情報科学的に新しい概念を生物学に導入していく事が分野の隆盛を支えるものである。本BoFセッションでは、特に後者に着目して、情報科学の最前線で研究を進めている研究者や、先端的な情報科学的手法をバイオインフォマティクスに応用してきた研究者らに講演していただき、具体的にどのような新しいバイオインフォマティクスが切り開けるか、また実際に応用するさいに気をつけるべき点などについて議論したい。
・Model Learning meets Biology ー生物データの背後に潜む「構造」を情報科学で明らかにするー
浜田道昭(早稲田大学 理工学術院、産総研CBBD-OIL)
・ChemTS:深層学習とモンテカルロ木探索を用いた新規分子生成
津田宏治(東京大学 大学院新領域創成科学研究科、理化学研究所 革新知能統合研究センター、物質・材料研究機構 統合型材料開発・情報基盤部門)
・関数推定の理論に基づく深層学習の原理解析
今泉允聡(統計数理研究所)
・バイオインフォマティクスにも使える(かもしれない)コンピュータアーキテクチャ技術
高前田伸也(北海道大学 大学院情報科学研究科)
ゲノム解析へのグラフ構造の応用〜ゲノムグラフの今〜
座長:原薗陛正(東京大学)
ゲノムを情報科学的なグラフ構造として扱うことにより、個人の多様性を参照ゲノムに組み込めるようになり、膨大なゲノムデータに対してより高精度な解析が可能になることが期待されています。そのためNGS、ゲノム情報を対象としている研究者にとってゲノムグラフは今後重要になってくると考えられます。こうした状況のもと、2017年11月にゲノムグラフ研究会を立ち上げ、有志一同で論文輪読やハンズオン形式での技術調査を行っております。
本セッションではゲノムグラフ研究会における我々の取り組みを紹介するとともに、海外の先行研究や、現状ではどのような解析がゲノムグラフによって実現できるのかについて具体例を交えて取り上げます。更に、ゲノムグラフによって我々が行っている解析はどう変わるのでしょうか。NGS解析の将来像と、それに対する日本からのコントリビューションを含めて、アルゴリズム開発の最新の動向について議論します。
・ゲノムグラフとデータ統合
片山俊明(ライフサイエンス統合データベースセンター)
・未定
笠原雅弘(東京大学大学院新領域創成科学研究科)
・グラフ型リファレンスを利用したNGS解析~アライメントとバリアントコールを概観する
鈴木創(東京大学大学院新領域創成科学研究科)
・MoMIG: グラフゲノムブラウザ
横山稔之、坂本祥駿、関真秀、鈴木穣、笠原雅弘(東京大学大学院新領域創成科学研究科)
・メタゲノムデータを用いたゲノムグラフ構築パイプラインの開発
大和田周甫、山田拓司(東京工業大学 生命理工学院)
質量情報から生物情報へ
質量分析インフォマティクス研究会 (座長:山本博之・ヒューマン・メタボローム・テクノロジーズ株式会社、吉沢明康・京都大学大学院薬学研究科)
メタボロームまたはプロテオームデータを得るためには、一般に質量分析法が用いられており、質量分析はNGSと並んでオミクス解析に於ける主要な測定手法としての地位を確立している。質量分析を用いて得られる質量情報から生物情報を導き出すためには、そのデータを情報科学的手法を用いて解析を行う質量分析インフォマティクスが必要不可欠である。本セッションでは、質量分析からどのような情報が得られるかについての基礎的な内容から始め、プロテオミクスでの質量分析データの解析手順、ソフトウェアを用いた実演を通してメタボロミクスでの解析手順を紹介すると共に、最近のホットトピックである代謝物の構造推定問題に対し、ネットワーク解析、ケモインフォマティクス、物理化学計算を用いたアプローチを紹介する。質量分析データ処理の基本から最新の話題までを一連の研究の流れに沿って紹介することで、日本に於けるこの分野の研究の一層の拡大発展に資することを目標とする。
・質量分析法 meets ゲノム情報
吉沢明康(京都大学大学院薬学研究科)
・質量分析を用いたメタボロミクス研究に必要なインフォマティクス
津川裕司(理化学研究所環境資源科学研究センターメタボローム情報研究チーム、理化学研究所生命科学研究センターメタボローム研究チーム )
・質量情報から構造情報を読み解く
早川英介(沖縄科学技術大学院大学)
・物理化学計算によるタンデム質量分析からの代謝物構造推定の取り組み
田中弥(ヒューマン・メタボローム・テクノロジーズ株式会社)
スポンサードセッション
スポンサー:国立研究開発法人 日本医療研究開発機構(AMED)
生命医薬情報学領域における倫理的・法的・社会的課題(ELSI)を考える
座長: 長神 風二(国立大学法人 東北大学 東北メディカル・メガバンク機構)
勝井 恵子(国立研究開発法人 日本医療研究開発機構 基盤研究事業部 バイオバンク課)
国立研究開発法人日本医療研究開発機構(AMED)は、わが国における医療分野の研究開発および環境整備の中核的役割を担う公的機関として2015年4月に設立された。設立以来、医療研究開発の成果を患者さんやご家族のもとに一刻も早く届けるべく、基礎から実用化まで一貫した医療研究開発の推進を図っている。それと同時に、患者さん一人一人に寄り添い、患者さんの「LIFE(生命・生活・人生)」を支えることをミッションとするAMEDは、医学研究における倫理審査体制や研究参加者保護の体制の強化のみならず、先端生命科学や医療研究開発にまつわるELSI(Ethical, Legal and Social Issues:倫理的・法的・社会的課題)に関する研究プログラムについても、重要な取組と位置づけ、支援を行っている。
そこで本セッションでは、先端生命科学や医療研究開発にまつわるELSIに関して取り組む若手研究者に、それぞれが従事するELSI研究についてご報告いただいたうえで、フロアとの議論を交えながら、生命医薬情報学領域におけるELSI について考察を深めることにしたい。
・病院併設型の研究基盤(バイオバンク)で経験するELSI課題
森田 瑞樹(国立大学法人 岡山大学 大学院医歯薬学総合研究科)
演者は現在,大学病院に設置された「岡山大学病院バイオバンク(略称:岡大バイオバンク)」の運営と実務に携わっている。私たちのバイオバンクは医歯薬分野を中心とした研究開発を支援する研究基盤であり,今後は様々な疾患の大規模なオミックス解析に関与する機会も増えていくことが想定される。
私たちのような病院の中に設置されたバイオバンクでは,自ら同意説明をし,手術室や検査室などから検体を回収するなど,臨床現場との接点が多い。こうした環境では,倫理指針には書かれていないようなELSIに関わる様々な問題を日常的に経験しており,その一部は矛盾や利害の衝突を伴う。
こうした現場での経験に基づいた3つの話題「プライバシーリスク」「同意とカストディアンシップ」「ダイナミックコンセント」について紹介する。臨床検体から生まれたデータの裏ではどのようなELSIの課題と向き合っているのかを知って頂き,生命医薬情報学の研究者のみなさんにも一緒に解決策を考えて頂くことを期待している。
・ゲノム解析研究における偶発的所見/二次的所見を含む個人の遺伝情報の結果返却に関するELSI
相澤 弥生(国立大学法人 東北大学 東北メディカル・メガバンク機構 広報・企画部門)
ゲノム解析技術の進歩により、全ゲノム/エクソーム解析等において、ゲノムを網羅的に解析することが可能となった。網羅的なゲノム解析では、目的とする所見である一次的所見だけではなく、本来の目的とは関係しない所見である偶発的所見/二次的所見(IF/SF)も同時に明らかにされることがある。そのため、そうした結果を解析対象者へ返却すべきなのか、またどのような所見をどのような手続きで返却すればよいのかといったことが世界中で議論となっている。
様々な議論の中で特に世界中の注目を集めたのが、米国臨床遺伝・ゲノム学会が2013年に発表した臨床における解析の際のIF/SFに関する推奨であり、ここでは返却すべき疾患のリストも示されている(当初は56遺伝子24疾患であったが、2016年に59遺伝子27疾患に改定)。
臨床現場で診断目的に行われた遺伝学的検査については、医療者と患者の間でインフォームド・コンセントや診療の中での十分なコミュニケーションが可能であること、医療というサービスの中で行われることなどから、国内外で、診断目的の所見以外の二次的所見について返却する取り組みが増えてきている。
しかし、研究の場合、特に基礎研究においては、臨床とは状況が異なり、様々な視点からELSIについて検討する必要がある。ACMGの推奨以降の海外の動向、我が国における状況などについて紹介したい。
・ヒトデータを用いる医学系研究における倫理的・法的手続きと、個人情報の保護について
山本 奈津子(国立大学法人 大阪大学 データビリティフロンティア機構)
ゲノム医療をはじめとする先端医療・医学研究開発においては、患者や健常者の研究への関わり方について考えることがますます重要になっている。研究参加者にどのような形で参加してもらうか、どのように説明し同意を取得するのか、どのように成果を還元していくのかといった点は、倫理的・法的・社会的な観点でのみ重要なのではなく、科学的な成果が得られるかといった結末までも左右する可能性がある。さらに近年では、研究参加者の試料や情報に対して、利用や処分に関する権利を持つのは誰かといった所有権的な概念の変化も生じており、研究を継続することについて様々な考慮や工夫が必要なこともある。
本発表ではまず、研究参加者を募る(あるいはヒトのデータを利用する)医学系研究を始める研究者が最初に行うべき倫理的・法的な手続きについて、短く解説する。
次に、研究者が倫理的・法的な不安を抱くことなく安全にヒトのデータを取り扱うために必要な知識として、特に近年のパーソナルデータに関する考え方の変化に注目し、研究で使われる臨床データ、ゲノムデータ、オミクスデータなどと、そのデータ主体(個人)の権利との関係について説明する。その際、2015年に改正され2017年に施行された個人情報保護法、EUの一般データ保護規則(EUにおける個人情報保護法、GDPR)、研究倫理指針を遵守する際に、研究者が留意すべき点についても概説する。
・再生医療を提供するクリニックのWebサイト情報と規制の動向
八田 太一(国立大学法人 京都大学 iPS細胞研究所 上廣倫理研究部門)
幹細胞生物学の進展と細胞の培養・保存にかかる技術の発展により、細胞治療への期待が高まる一方で、科学的根拠の乏しい細胞治療が提供される事例も報告されている。科学性を装い患者さんの期待を逆手にとったWebサイトの存在は世界中で問題となっている。細胞治療という発展途上の治療にアクセスする際、患者が必要な情報を取捨選択することは容易ではない。
内閣府消費者委員会の調べでは、近年、美容医療サービスに関する消費者トラブルの相談件数が増加したこと、トラブルのきっかけがWebサイトであると報告されている。これを受けて、平成29年6月、「医療法」が部分改正され、病院やクリニックのWebサイトが医療広告規制の対象となり、これらのWebサイトの監視体制が強化された。これによって誇大な広告が規制され、より適切な情報が提供されるように方向づけられると予想される。しかし、患者の期待と誤解は表裏一体であるとも言える。そのことを踏まえると、広告規制のみでWebサイトを介したトラブルのすべてを解決することは困難であろう。
我々の調査グループでは、平成29年に「医療法」が部分改正される以前より、細胞治療を提供する自由診療クリニックのWebサイトを収集し、Webサイト情報の質評価を実施した。本発表では、その調査の一端を紹介し規制の動向を示すことで、生命医薬情報学領域における倫理的・法的・社会的課題を論じたい。
・フロア・ディスカッション:生命医薬情報学領域におけるELSI研究の重要性
スポンサー:オックスフォード・ナノポアテクノロジーズ
オックスフォード・ナノポアシークエンスのデータ解析と応用
・「オックスフォード・ナノポアシークエンサーから出てくるデータと様々な解析ツール」
宮本 真理(株式会社オックスフォード・ナノポアテクノロジーズ)
オックスフォード・ナノポアテクノロジーズは、小さな穴を持ったナノポアタンパク質の穴を通る分子を電流の変化として測定しディープラーニングを使ったベースコーラーで塩基配列を取得している。従来のNGSデータとは違い非常に長いリードが得られることが大きな特徴であり、従来のNGS解析とは異なる解析ツールが使われることが多い。本セッションでは基本的な原理から、取得されるデータの種類とナノポアで提供しているベースコーラーや解析ツールの紹介、オープンソースで提供されている様々な解析ツールを通じて、どのような解析が可能か、それらを使った論文紹介を交えて話をするとともに、今後の開発予定についても紹介する。
・「ヒト遺伝性疾患の原因を見つけるための、ロングリードの解析ツール」
三橋 里美(横浜市立大学)
Martin C Frith(AIST・東京大学)
ヒト遺伝性疾患の原因を知るためには、従来のショートリードのNGSが広く用いられ、一定の成果を上げてきた。しかし、未だ、7割以上の患者では、原因となる変異を同定することは難しい。この原因は様々だが、ショートリードでは解析困難な領域に変異がある場合、ロングリードシークエンサーが、解決の突破口となるかもしれない。私たちは、LAST alignerを用いて、リピート領域やゲノム構造異常などを検出するための、ロングリードの解析に有用なツールを開発し、実際に患者に見られる変異を見出している。これらのツールの紹介と、開発の状況を紹介したい。
スポンサー:国立研究開発法人科学技術振興機構
フィールドに向かう植物科学とインフォマティクスの接点
永野惇(龍谷大学農学部)
植物科学においても、分子生物学的な解析手法の進展によって、環境応答をはじめとする様々なシステムの分子基盤が急速に明らかになってきた。それにともなって、植物科学の成果を実際の農業や生産現場での問題解決や温暖化等の環境変動からの影響の予測に用いることが強く望まれるようになってきている。しかしながら、単純な実験室環境下で行われてきた分子生物学的解析の結果を、時空間的に複雑に変動する野外(フィールド)における現象にそのまま当てはめることは困難である。実際には、植物科学のみならず、農学、情報科学、工学など多様な分野との協働によって、総合的な取り組みが求められている。そこには、オミクスデータから、画像データ、気象データ、場合によっては流通データまで、広範かつヘテロなデータを取り扱う必要があり、当然、生物学的、情報科学的チャレンジがある。このような分野へのバイオインフォマティクス学会からの参入を期待してセッションを企画した。当日は、関連する科学技術振興機構 CREST「環境変動に対する植物の頑健性の解明と応用に向けた基盤技術の創出」研究領域、さきがけ「フィールドにおける植物の生命現象の制御に向けた次世代基盤技術の創出」研究領域、さきがけ「情報科学との協働による革新的な農産物栽培手法を実現するための技術基盤の創出」研究領域の3領域から5名の演者が講演を行う。
・野外におけるトランスクリプトーム変動を予測する
永野惇(龍谷大学農学部)
・野外農生態系の理解・予測・制御に向けた生物群集の動態捕捉と時系列解析
潮雅之(JSTさきがけ、京都大学生態学研究センター)
・生物情報学的手法による複雑な花粉識別システムの理解
藤井壮太(東京大学大学院農学生命科学研究科、JSTさきがけ)
・大規模圃場における作物個体の生育モニタリング
杉浦綾(農研機構 北海道農業研究センター)
・モデルベース開発(MBD)で植物新品種開発を一変させる
岩田洋佳(東京大学大学院農学生命科学研究科)
スポンサー:株式会社ナベインターナショナル
計算機インフラ企業から見る大規模バイオメディカルデータ解析の潮流
渡辺理恵(株式会社ナベ インターナショナル マーケティング部)
実験や計測、医療など各機器の高性能化に従い、産出されるデータ量は爆発的に増えている。また、大量の画像やテキストを対象にディープラーニングなど人工知能の手法を適用する研究が、生物医学分野においても盛んになっている。一方、クラウドなどウェブベースの技術を中心とした商用コンピューティングにおいて、リレーショナルデータベースに整然と蓄積されない、いわゆるビッグデータ解析の盛り上がりが年々大きくなっている。このような中、ビッグデータ解析を中心とした商用コンピューティング技術を生物医学研究へ導入することにより、新しい手法へ可能性の広がりが期待できる。本セッションでは、バイオメディカルデータ解析を支えるコンピューティングエンジニアリング寄りの技術について、最新の動向をいくつか紹介する。また、海外や国内、弊社お客様の事例も含めた大規模データ処理の潮流を俯瞰し、計算機インフラ企業の視点から分析したい。そして、機械学習、グラフ解析、ストリーミング解析等を可能とする分散処理フレームワークApache Spark、およびApache Sparkを構築済みとしたナベ インターナショナルの生物医学研究向け大規模データ解析環境Takeru Elysiaを紹介する。
スポンサー:株式会社メタジェン
消化器難病疾患に対する便細菌叢移植療法 ~腸内細菌叢制御による疾患治療と今後の展望~
石川大(株式会社メタジェン・順天堂大学医学部消化器内科学講座)
難病指定疾患「潰瘍性大腸炎」。1時間ごとに繰り返される頻回の下痢、血便、激しい腹痛に多くの患者が苦しんでおり、直近10年間でその患者数はほぼ2倍の約19万人と急増し、その高額な治療費の増加も大きな医療財政上の問題となっている。こういった背景から新しい治療戦略として、患者の腸内細菌叢に積極的に介入する「便細菌叢移植療法(通称:便移植)」に注目が集まっている。 便移植は、健康なドナーの腸内細菌叢を患者の大腸内に内視鏡を使って移植するというシンプルかつ原始的な治療方法であるが、長期の抗生剤投与によって発症する偽膜性腸炎に対する高い治療効果が証明され、欧米では既に実用化されている。この治療方法を潰瘍性大腸炎に応用できないか?そして急増する患者の新規治療になり得るか?この課題に取り組むため、2014年7月に順天堂大学消化器内科学講座腸内細菌研究グループでは、世界に先駆けて潰瘍性大腸炎患者対し、便移植と抗生剤治療とを組み合わせた新規腸内細菌叢移植療法の確立を目指し、臨床研究を開始した。約4年間で140名の患者が参加し、その治療効果が見えてきた。本発表では、便移植による臨床経過と、患者の腸内細菌叢の解析を通して明らかとなったこと、さらにはそのメカニズムや今後の可能性について紹介する。加えて、メタジェンで展開する腸内細菌治療の可能性や、将来展望についても熱い意見を交わしたい。
・質疑・パネルディスカッション
登壇者:石川 大(株式会社メタジェン・順天堂大学医学部付属順天堂医院消化器内科学講座)
福田真嗣(株式会社メタジェン・慶應義塾大学先端生命科学研究所)
山田拓司(株式会社メタジェン・東京工業大学生命理工学院)
ランチョンセミナー
スポンサー:アマゾン ウェブ サービス ジャパン株式会社 2018年9月19日(水)
・AWS概要と研究分野における事例
アマゾン ウェブ サービス ジャパン株式会社
AWSは様々なエリアでゲノム解析を含む様々なエリアで利用されているクラウドサービスです。AWSで利用可能な最新技術と日本及び諸外国の事例をご紹介いたします。
スポンサー:日本蛋白質構造データバンク(PDBj) 2018年9月20日(木)
・PDBjとwwPDBの活動方針について
栗栖 源嗣 (大阪大学蛋白質研究所)
PDBj (Protein Data Bank Japan, https://pdbj.org/)は,worldwide PDB(wwPDB, https://wwpdb.org/)のメンバーとして国際的な共同作業により,蛋白質等の生体高分子の構造を登録し,PDB(Protein Data Bank)データとして座標と実験データを全世界へ無償で公開しています.今回のセミナーでは,wwPDBで行ってきた厳しい品質管理と構造データに対する検証レポートの充実・RDF化について紹介します.更に,2017年10月に導入されたバージョンを付した新しいPDB IDの情報を含め,最近の活動内容をご紹介いたします.
・Introduction to PDBj services for searching and exploring the PDB
BEKKER, Gert-Jan (大阪大学蛋白質研究所)
In this seminar, we will introduce the PDBj Mine search system, including the SQL search functionality and the corresponding REST APIs. PDBj also offers a full dump file of the PostgreSQL RDB on our ftp site, which users can load on their local machine. We will show how searching the PDB using keywords/metadata, sequence and structure works, and how one can view the three dimensional structure using our web-based molecular viewer, Molmil. We also offer an RDF service, which has been integrated into the NBDC RDF Portal, linking many databases together with the PDB. Finally, we will also show how Molmil can be used to visualize Molecular Dynamics trajectory data and how Molmil can be scripted.
一般口頭発表I
日時・会場:9月19日(水) 13:30-15:00 タクト大ホール
座長:佐藤昌直(北海道大学農学研究院基礎研究部門)
・個人ゲノム情報に基づくヒト顔形状の予測をめざして
今西規1、中川草1、木村亮介2、瀧靖之3、安藤寿康4(1. 東海大学医学部、2. 琉球大学大学院医学研究科、3. 東北大学加齢医学研究所、4. 慶應大学文学部)
・Development of genome variant annotation system with protein 3D structures and applications to variants in Japanese population
Matsuyuki Shirota (Tohoku University)
・放線菌ロドコッカス属における遺伝子配列改変による発現調節の解析
Naoyuki Tajima, Wataru Kitagawa, Yutaka Saito, Yoshiyuki Nishimiya, Kouichi Tamano, Yoshiaki Yasutake, Tomohiro Tamura, Tomoshi Kameda (National Institute of Advanced Industrial Science and Technology (AIST))
・Pan-cancer module network analysis for identifying dominating networks across human cancers
Chun-Yu Lin1, Jinn-Moon Yang2, Tatsuya Akutsu1, (1. Kyoto University, 2. National Chiao Tung University)
一般口頭発表
一般口頭発表I
日時・会場:9月19日(水) 13:30-15:00 タクト大ホール
座長:佐藤昌直(北海道大学農学研究院基礎研究部門)
・個人ゲノム情報に基づくヒト顔形状の予測をめざして
今西規1、中川草1、木村亮介2、瀧靖之3、安藤寿康4(1. 東海大学医学部、2. 琉球大学大学院医学研究科、3. 東北大学加齢医学研究所、4. 慶應大学文学部)
・Development of genome variant annotation system with protein 3D structures and applications to variants in Japanese population
Matsuyuki Shirota (Tohoku University)
・放線菌ロドコッカス属における遺伝子配列改変による発現調節の解析
Naoyuki Tajima, Wataru Kitagawa, Yutaka Saito, Yoshiyuki Nishimiya, Kouichi Tamano, Yoshiaki Yasutake, Tomohiro Tamura, Tomoshi Kameda (National Institute of Advanced Industrial Science and Technology (AIST))
・Pan-cancer module network analysis for identifying dominating networks across human cancers
Chun-Yu Lin1, Jinn-Moon Yang2, Tatsuya Akutsu1, (1. Kyoto University, 2. National Chiao Tung University)
一般口頭発表II
日時・会場:9月19日(水) 13:30-15:00 タクト練習室
座長:鈴木治夫(慶應義塾大学先端生命科学研究所)
・公共データベースの顕微鏡画像を用いた細胞核分裂の定量計測と表現型解析
遠里由佳子1、岡田初美2、京田耕司2、大浪修一2 (1. 大阪電気通信大学 情報通信工学部 情報工学科、2. 理化学研究所 生命機能科学研究センター 発生動態研究チーム)
・脂肪由来幹細胞(Adipose-derived stem cell)の分化に関与するエピジェネティック因子の探索
山谷恭代1,2、朴聖俊2、中井謙太1,2 (1. 東京大学新領域創成科学研究科メディカル情報生命専攻、2. 東京大学医科学研究所)
・A comprehensive analysis of the effects of alternative splicing on RNA localization in human
Chao Zeng, Michiaki Hamada (Waseda University)
・ヒトのエンハンサーと遺伝子相互作用や転写制御に影響する、方向性のある転写因子DNA結合配列の発見
大里直樹 (大阪大学大学院情報科学研究科バイオ情報工学専攻)
一般口頭発表III
日時・会場:9月19日(水) 15:15-16:45 アートフォーラム会議室
座長:山田拓司(東京工業大学大学院生命理工学研究科)
・木構造棒折り過程によるIRMの階層化と生命情報解析への応用
宮原雅人、浜田道昭 (早稲田大学 / 早大・産総研CBBD-OIL)
・Logicome Profiler: 統計的に有意な遺伝子三項間論理関係の同定法
Tsukasa Fukunaga, Wataru Iwasaki (The University of Tokyo)
・Cyclic attractor estimation in Boolean networks
Ulrike Münzner1, Edda Klipp2, Marcus Krantz2, Tatsuya Akutsu1 (1. Kyoto University, 2. Humboldt-Universität zu Berlin)
・非負値テンソル分解を用いた細胞間コミュニケーションの検出
露崎弘毅、石井学、二階堂愛 (理化学研究所 生命機能科学研究センター バイオインフォマティクス研究開発ユニット)
一般口頭発表IV
日時・会場:9月19日(水) 15:15-16:45 タクト練習室
座長:斎藤 輪太郎(慶應義塾大学先端生命科学研究所)
・サンプル環境の再構成による遺伝子共発現情報の種間比較可能性の向上
大林武 (東北大学)
・TimeXNet Web: Identifying cellular response networks from diverse time-course omics profiles
Phit Ling Tan1, Yosvany López2, Kenta Nakai1, Ashwini Patil1 (1. Human Genome Center, The Institute of Medical Science, The University of Tokyo, 2. Department of Medical Science Mathematics, Medical Research Institute, Tokyo Medical and Dental University)
・LC/MS/MSマススペクトログラムの階層クラスタリングに基づくタンパク質同定
Koki Kibe, Akiyasu.C Yoshizawa, Tsuyoshi Tabata, Kazuyoshi Yoshii, Yasushi Ishihama (Kyoto University)
・相互作用パターン抽出による生物種ワイドな相互作用予測法の開発
白石慧、奥田利美、宮坂奈津子、大杉知裕、佐竹炎 (公益財団法人サントリー生命科学財団 生物有機科学研究所)
一般口頭発表V
日時・会場:9月20日(木) 10:45-12:15 アートフォーラム会議室
座長:大上雅史(東京工業大学 情報理工学院 情報工学系)
・真核生物ゲノムに内在化したウイルス様配列データベースgEVEを活用したトランスクリプトーム解析
中川草1、上田真保子2、Kirill Kryukov1、三橋里美3、三橋弘明4、今西規1 (1. 東海大学医学部 分子生命科学、2. 東海大学マイクロ・ナノ研究開発センター、3. 横浜市立大学大学院医学研究科 遺伝学、4. 東海大学工学部 生命化学科)
・A novel deep learning method for pathological diagnosis of malignant melanoma.
Yuji Ota, Kosuke Shido, Kaname Kojima, Masao Nagasaki, Kenshi Yamasaki, Setsuya Aiba (Tohoku University)
・Three-Dimensional Chromatin Structures Coordinate with Gene Expression Levels and Reveals Inter-chromosomal Interactions in B-Cell Lymphoma
Luis A. E. Nagai1, Sung-Joon Park2, Kenta Nakai2 (1. Department of Computational Biology and Medical Science, the University of Tokyo, 2. Human Genome Center, the Institute of Medical Science, the University of Tokyo)
・人工知能を使って乳がん患者の生存予後を正確に予測する
Hideyuki Shimizu, Keiichi Nakayama (Kyushu University)
一般口頭発表VI
日時・会場:9月20日(木) 10:45-12:15 タクト練習室
座長:志水厚志(岩手医科大学 いわて東北メディカル・メガバンク機構)
・Graph Splitting Method Resolves the Early Evolution of Protein Superfamilies
Motomu Matsui, Wataru Iwasaki (The University of Tokyo)
・いわて東北メディカル・メガバンク機構におけるゲノム・オミックス解析研究と個別化予防の実現への取り組み
Atsushi Shimizu, Hideki Ohmomo, Shohei Komaki, Yoichi Sutoh, Ryohei Furukawa, Yuh Shiwa, Tsuyoshi Hachiya, Makoto Sasaki (Iwate Medical University)
・ゲノム・コホート研究における疫学者とバイオインフォマティシャンの共同研究の現状と課題
須藤洋一、八谷剛史、小巻翔平、大桃秀樹、清水厚志 (岩手医科大学 いわて東北メディカル・メガバンク機構 生体情報解析部門)
・代謝系の動的特性解析のための速度モデルにおける大過剰化合物の有無の影響
Daisuke Tominaga1, Hideo Kawaguchi2, Yoshimi Hori2, Tomohisa Hasunuma2, Chiaki Ogino2 (1. National Institute of Advanced Industrial Science and Technology (AIST), 2.Kobe University)